Este jueves, la FDA analiza la posible aprobación de la vacuna Pfizer
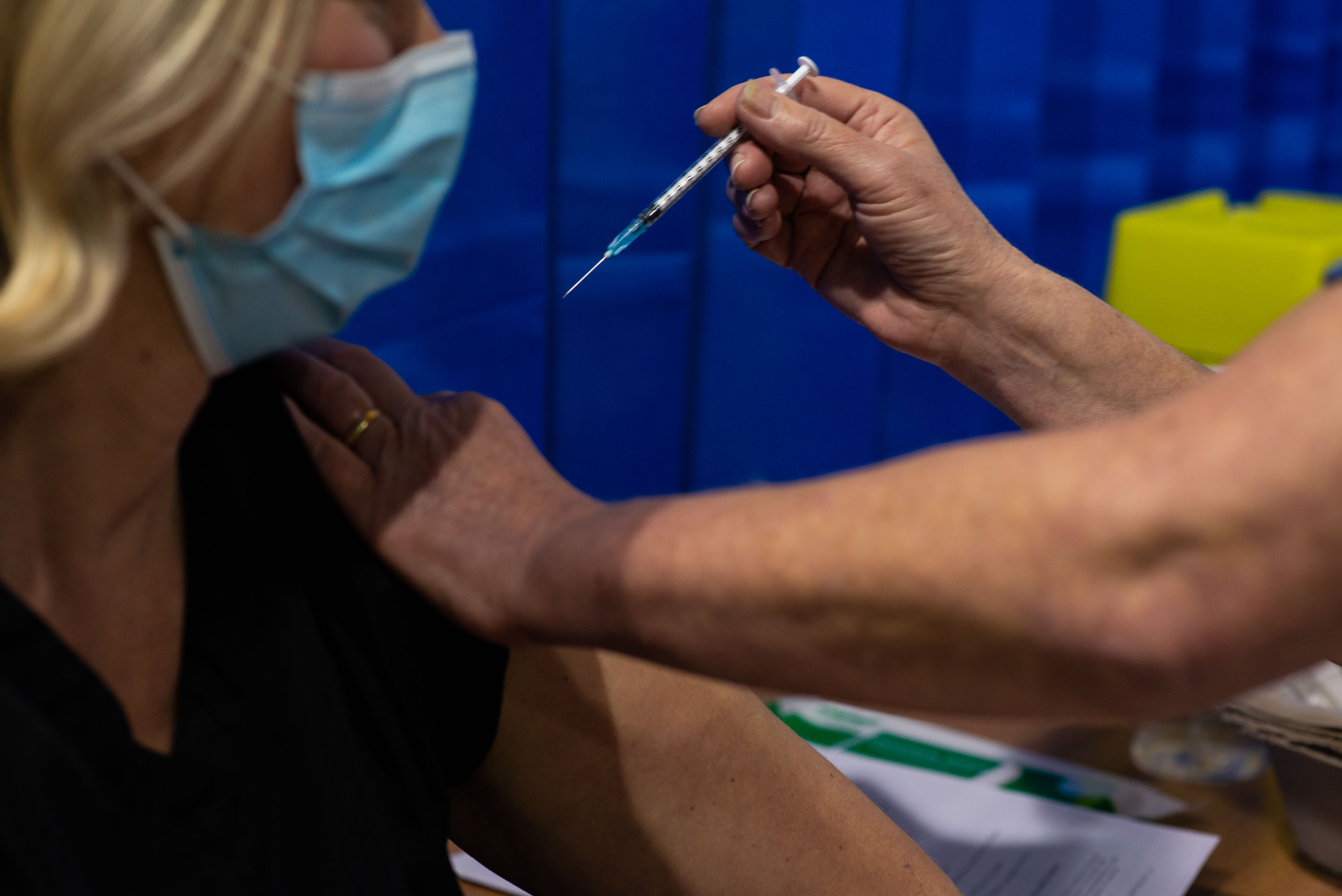
(CNN) – La Administración de Drogas y Alimentos de los Estados Unidos (FDA) revisará la autorización de uso de emergencia para la vacuna candidata Pfizer y BioNTech para el covid-19 el jueves después de que un comité asesor publicara un documento de información sobre esa vacuna el martes.
El documento confirma que la efectividad de la vacuna COVID-19 fue del 95%, ocurriendo al menos siete días después de la segunda dosis, eficacia ya reportada por Pfizer. El régimen de dosificación propuesto para la vacuna es administrar dos dosis de 30 microgramos con 21 días de diferencia.
Sin embargo, el documento también señala que la vacuna, llamada BNT162b2, parece brindar «cierta protección» contra COVID-19 después de una sola dosis.
El documento describe la efectividad de la vacuna Pfizer en el tiempo entre la primera y la segunda dosis como 52.4%, pero el documento señala que “la eficacia observada después de la dosis 1 y antes de la dosis 2, ya que un análisis post-hoc no puede apoyan una conclusión sobre la eficacia de una sola dosis de la vacuna, porque el tiempo de observación está limitado por el hecho de que la mayoría de los participantes recibieron una segunda dosis después de tres semanas. ‘
En otras palabras, «el estudio no contó con un brazo de dosis única para hacer una comparación adecuada».
Detalles de la vacuna que está siendo evaluada por la FDA
El documento continúa detallando el perfil de seguridad de la vacuna como «favorable» y señala que las reacciones adversas más comunes a la vacuna fueron reacciones en el lugar de la inyección, fatiga, dolor de cabeza, dolor muscular, escalofríos, dolor articular y fiebre.
Las reacciones adversas graves ocurrieron en menos del 4,6% de los participantes, fueron más comunes después de la segunda dosis y, en general, fueron menos comunes en los adultos mayores que en los participantes más jóvenes, según el artículo. El documento agrega que el aumento de los ganglios linfáticos también puede estar relacionado con la vacunación.
En general, «actualmente no hay datos suficientes para sacar conclusiones sobre la seguridad de la vacuna en subpoblaciones como niños menores de 16 años, embarazadas y lactantes e inmunosuprimidos», según el artículo.
Un total de seis participantes murieron durante las pruebas y «todas las muertes representan eventos que ocurren en la población general de los grupos de edad en los que ocurrieron, a una tasa similar».
El documento se discutirá en una reunión el jueves, donde el Comité Asesor de Vacunas y Productos Biológicos Relacionados de la FDA proporcionará recomendaciones a la FDA sobre si la vacuna es eficaz para prevenir el covid-19 en personas de 16 años de edad o más y si los beneficios potenciales de la vacuna superan los riesgos.
«El comité también discutirá qué estudios adicionales debe realizar el fabricante de la vacuna después de emitir la autorización de uso de emergencia para recopilar más datos sobre la seguridad y eficacia de esta vacuna», según el documento.
Están destinados a administrar la vacuna dentro de las 96 horas posteriores a la autorización.
Las vacunas Covid-19 se distribuirán a las poblaciones vulnerables a los pocos días de un permiso de uso de emergencia, dijo un funcionario, mientras Estados Unidos lucha con un registro histórico de nuevos casos diarios.
«Comenzaremos a recibir disparos dentro de las 96 horas posteriores a la autorización de uso de emergencia», dijo el martes el general Gustave Perna, director de operaciones de Operation Warp Speed. «Esto es lo que creo con todo mi corazón».
Pfizer y Moderna tienen candidatos a vacunas pendientes de autorización para uso de emergencia, y la FDA confirmó la seguridad y eficacia de Pfizer antes de la reunión de aprobación del jueves. La aprobación temprana ocurre cuando EE. UU. Sufre picos en casos de coronavirus, hospitalizaciones y muertes.
Estados Unidos ha registrado un promedio de 206,152 nuevos casos por día durante los últimos siete días, el número más alto de casos pandémicos hasta la fecha. Y el martes, 104-600 personas fueron hospitalizadas con el virus, según The COVID Tracking Project, un récord que se ha establecido y batido varias veces en las últimas semanas. En total, más de 286.000 personas murieron a causa del virus y más de 15,1 millones se infectaron, según datos de la Universidad Johns Hopkins.
El público en general probablemente tendrá que seguir luchando con el pico de la temporada navideña hasta que las vacunas estén ampliamente disponibles en 2021. Pero los funcionarios se apresuran a distribuir las vacunas en los próximos días a las poblaciones prioritarias: los ancianos y los trabajadores. de salud.
Aunque es una «tarea hercúlea», Perna dijo que confía en que, con la planificación de los CDC y la colaboración de los socios, «seremos capaces de entregar esta vacuna de manera muy eficiente, pero lo más importante, de manera efectiva». .
Con información de Madeline Holcombe y Jacqueline Howard




