El equipo mide la ruptura de un solo enlace químico
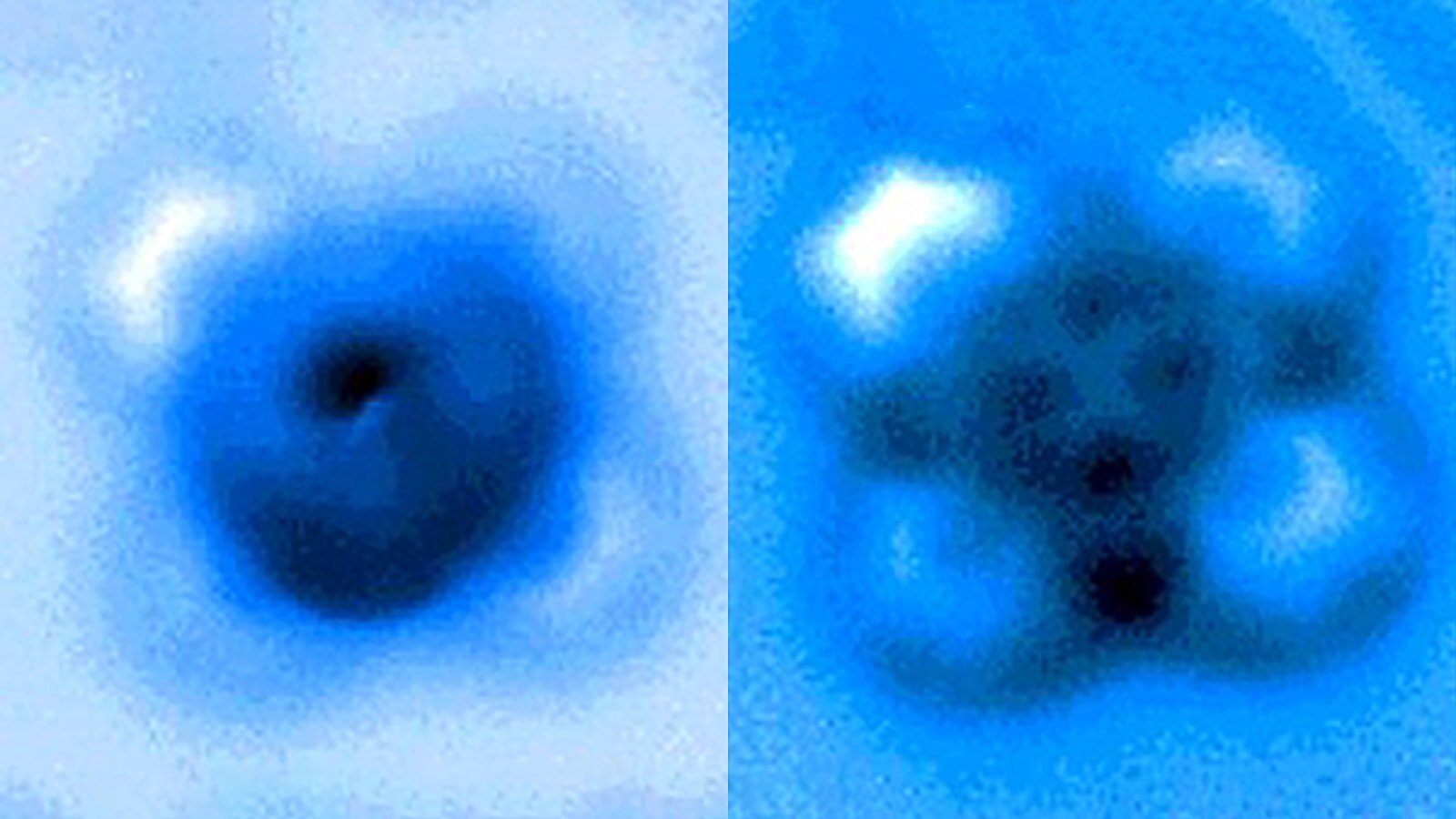
Los investigadores midieron las fuerzas mecánicas aplicadas para romper un enlace entre el monóxido de carbono y la ftalocianina de hierro, que aparece como una cruz simétrica en las imágenes de microscopía de sonda de barrido tomadas antes y después de la rotura del enlace. Crédito: Pengcheng Chen et al.
El equipo utilizó un microscopio de fuerza atómica de alta resolución (AFM) que operaba en un entorno controlado en el Centro de Análisis e Imágenes de Princeton. La sonda AFM, cuya punta termina en un solo átomo de cobre, se acercó gradualmente al enlace hierro-carbono hasta que se rompió. Los investigadores midieron las fuerzas mecánicas aplicadas en el momento de la rotura, que eran visibles en una imagen capturada por el microscopio. Un equipo de la Universidad de Princeton, la Universidad de Texas-Austin y ExxonMobil informó los resultados en un artículo publicado el 24 de septiembre en Comunicaciones de la naturaleza.
«Es una imagen asombrosa: poder ver realmente una sola molécula pequeña en una superficie con otra adherida a ella es asombroso», dijo el coautor Craig Arnold, profesor de Ingeniería Mecánica y Aeroespacial Susan Dod Brown y director del Instituto de Princeton. para Ciencia y Tecnología de Materiales (PRISM).
«El hecho de que podamos caracterizar Enlace, tanto tirar como empujar, nos permite comprender mucho más sobre la naturaleza de estos tipos de enlaces, su fuerza, cómo interactúan, y eso tiene todo tipo de implicaciones, especialmente para la catálisis, donde tienes una molécula en una superficie y entonces algo interactúa con ella y hace que se derrumbe «, dijo Arnold.
Nan Yao, el investigador principal del estudio y director del Centro de Análisis e Imágenes de Princeton, señaló que los experimentos también revelaron información sobre cómo la ruptura de enlaces afecta las interacciones de un catalizador con la superficie en la que está adsorbido. Mejorar el diseño de catalizadores químicos tiene relevancia para la bioquímica, la ciencia de los materiales y las tecnologías energéticas, agregó Yao, quien también es profesor de práctica e investigador principal en PRISM.
En los experimentos, el átomo de carbono era parte de una molécula de monóxido de carbono y el átomo de hierro era ftalocianina de hierro, un pigmento común y un catalizador químico. La ftalocianina de hierro está estructurada como una cruz simétrica, con un solo átomo de hierro en el centro de un complejo de anillos conectados a la base de nitrógeno y carbono. El átomo de hierro interactúa con el carbono en el monóxido de carbono, y el hierro y el carbono comparten un par de electrones en un tipo de enlace covalente conocido como enlace dativo.
Yao y sus colegas utilizaron la punta de la sonda a escala atómica del instrumento AFM para romper el enlace hierro-carbono, controlando con precisión la distancia entre la punta y las moléculas unidas, en incrementos de 5 picómetros (5 mil millonésimas de milímetro). La ruptura ocurrió cuando la punta estaba 30 picómetros por encima de las moléculas, una distancia que es aproximadamente una sexta parte del ancho de un átomo de carbono. En este punto, la mitad de la molécula de ftalocianina de hierro se ha vuelto más borrosa en la imagen AFM, lo que indica el punto de ruptura del enlace químico.
Los investigadores utilizaron un tipo de AFM conocido como sin contacto, en el que la punta del microscopio no entra en contacto directo con las moléculas en estudio, sino que utiliza cambios de frecuencia de vibración a escala fina para construir una imagen de la superficie de las moléculas.
Al medir estos cambios de frecuencia, los investigadores también pudieron calcular la fuerza necesaria para romper el enlace. Una sonda de cobre estándar rompió el enlace hierro-carbono con una fuerza atractiva de 150 piconewtons. Con otra molécula de monóxido de carbono unida a la punta, el enlace se rompió por una fuerza repulsiva de 220 piconewtons. Para investigar la base de estas diferencias, el equipo utilizó métodos de simulación cuántica para modelar cambios en las densidades de electrones durante reacciones químicas.
El trabajo aprovecha la tecnología AFM desarrollada por primera vez en 2009 para visualizar enlaces químicos simples. La rotura controlada de un enlace químico utilizando un sistema AFM ha sido más desafiante que estudios similares de formación de enlaces.
«Es un gran desafío mejorar nuestra comprensión de cómo se pueden llevar a cabo las reacciones químicas manipulando átomos, es decir, con la punta de un microscopio de barrido», dijo Leo Gross, que dirige el Grupo de Investigación de Manipulación de Átomos y Moléculas de IBM Research en Zurich, y fue el autor principal del 2009 estudio quien resolvió por primera vez la estructura química de una molécula por AFM.
Al romper un enlace particular con diferentes extremos que utilizan dos mecanismos diferentes, el nuevo estudio contribuye a «mejorar nuestra comprensión y control de la escisión de enlaces mediante la manipulación de átomos. Se suma a nuestra caja de herramientas para la química mediante la manipulación de átomos y representa un paso adelante hacia la fabricación de ingeniería moléculas de complejidad creciente «, agregó Gross, que no participó en el estudio.
Los experimentos son extremadamente sensibles a las vibraciones externas y otros factores de confusión. El instrumento especializado AFM del Centro de imágenes y análisis está alojado en un entorno de alto vacío y los materiales se enfrían a una temperatura de 4 Kelvin, solo unos pocos grados por encima del cero absoluto, utilizando helio líquido. Estas condiciones controladas producen mediciones precisas, asegurando que el moléculasLos estados e interacciones energéticos sólo se ven afectados por manipulaciones experimentales.
«Necesita un sistema muy bueno y limpio porque esta reacción puede ser muy complicada, con tantos átomos involucrado, es posible que no sepa qué vínculo romper en una escala tan pequeña «, dijo Yao. El diseño de este sistema simplificó todo el proceso y aclaró lo desconocido “al romper un enlace químico, dijo.
Los autores principales del estudio fueron Pengcheng Chen, investigador asociado de PRISM, y Dingxin Fan, estudiante de doctorado en la Universidad de Texas-Austin. Además de Yao, otros autores correspondientes fueron Yunlong Zhang de ExxonMobil Research and Engineering Company en Annandale, Nueva Jersey, y James R. Chelikowsky, profesor de UT Austin. Además de Arnold, otros coautores de Princeton fueron Annabella Selloni, profesora de química David B. Jones, y Emily Carter, profesora Gerhard R. Andlinger ’52 en Energía y medio ambiente. Otros coautores de ExxonMobil fueron David Dankworth y Steven Rucker.
Rompiendo un vínculo dativo con fuerzas mecánicas, Comunicaciones de la naturaleza (2021). DOI: 10.1038 / s41467-021-25932-6 , www.nature.com/articles/s41467-021-25932-6
Proporcionado por
Universidad de Princeton
Cita: El equipo mide la rotura de un enlace químico simple (2021, 4 de octubre) recuperado el 4 de octubre de 2021 en https://phys.org/news/2021-10-team-breakup-chemical-bond.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo para fines de investigación o estudio privado, ninguna parte puede ser reproducida sin permiso por escrito. El contenido se proporciona únicamente con fines informativos.